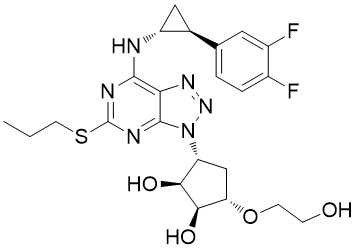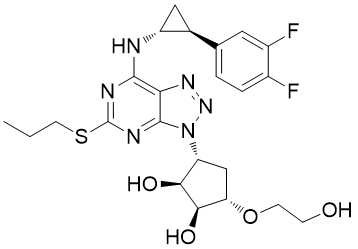
274693-27-5 api cardio-vasculaires C23H28F2N6O4S 619-540-9 de Ticagrelor
-
Surligner
274693-27-5 intermédiaires pharmaceutiques
,Intermédiaires pharmaceutiques d'api
,Intermédiaires pharmaceutiques cardio-vasculaires de Ticagrelor
-
Nom de produitTICAGRELOR
-
Synonymes1,2-Cyclopentanediol, 3 [7 [[(1R, 2S) - 2 cyclopropyl (3,4-difluorophenyl)] aminés] - 5 (propylthio)
-
CAS274693-27-5
-
MFC23H28F2N6O4S
-
MW522,57
-
EINECS619-540-9
-
Point d'ébullition°C 777.6±70.0 (prévu)
-
Densité1,67
-
Pureté98%
-
Lieu d'origineLA CHINE
-
Nom de marqueRUN
-
CertificationIOS9001
-
Numéro de modèleRUN-Z
-
Quantité de commande min10g
-
Prixinquiry
-
Détails d'emballage10g 50g 100g 500g 1kg
-
Délai de livraison3-7 jours
-
Conditions de paiementT/T, MoneyGram, BTCcoin
-
Capacité d'approvisionnement1kg --100kg
274693-27-5 api cardio-vasculaires C23H28F2N6O4S 619-540-9 de Ticagrelor
| Données de base de TICAGRELOR |
| Indications et mécanismes d'utilisation de recherche clinique d'action |
| Nom de produit : | TICAGRELOR |
| Synonymes : | 1,2-Cyclopentanediol, 3 [7 [[(1R, 2S) - 2 cyclopropyl (3,4-difluorophenyl)] aminés] - 5 (propylthio) - 3H-1,2,3-triazolo [4,5-d] pyrimidin-3-yl] - 5 (2-hydroxyethoxy) -, (1S, 2S, 3R, 5S) - ; Ticagrelor, >=98%; Ticagrelo ; Ticargrelor ; Brilinta ; Possia ; Ticagrelor et intermédiaires ; Normes de Ticagrelor |
| CAS : | 274693-27-5 |
| MF : | C23H28F2N6O4S |
| MW : | 522,57 |
| EINECS : | 619-540-9 |
| Catégories de produit : | AZD6140 ; Ticagrelor ; Composés aromatiques ; Heterocycles ; Intermédiaires et produits chimiques fins ; Api cardio-vasculaires ; Pharmaceutiques ; Composés de soufre et de sélénium ; Api |
| Mol File : | 274693-27-5.mol |
| Propriétés chimiques de TICAGRELOR |
| Point d'ébullition | °C 777.6±70.0 (prévu) |
| densité | 1,67 |
| pka | 13.26±0.70 (prévu) |
| Utilisation et synthèse de TICAGRELOR |
| Indications et utilisation | Ticagrelor, un nouvel inhibiteur d'agrégation de plaquette avec succès développé par AstraZeneca (États-Unis), est l'antagoniste de récepteur oral-administré la première par combinaison de diphosphate d'adénosine P2Y12 du monde réversible. Il est employé pour réduire la mort et des crises cardiaques cardio-vasculaires dans les patients présentant le syndrome coronaire aigu (ACS.) Le début rapide après administration par voie orale, et peut effectivement améliorer des symptômes des patients avec ACS. Thienopyridines est un inhibiteur P2Y12 réversible, ainsi il s'applique particulièrement vers les patients qui doivent subir la thérapie d'anticoagulant avant chirurgie. |
| Mécanismes d'action | Réversiblement les actes sur le sous-type P2Y12 de récepteur de la purine 2 (purinoceptor 2, P2,), des cellules musculaires lisses vasculaires (VSMC,) n'exige pas l'activation métabolique, et exerce un effet inhibiteur significatif sur l'agrégation de plaquette induite par le diphosphate d'adénosine (l'ADP.) |
| Recherche clinique | Ticagrelor a été approuvé par les États-Unis Food and Drug Administration (FDA) sur la base des études cliniques de PLATON. PLATON était 43 un pays, 862 le centre randomisé, l'étude à double anonymat et multi-centrée qui a inclus 18 624 patients hospitalisés pour ACS. Des patients ont été aléatoirement donnés aspirin plus le ticagrelor, ou aspirin plus le clopidogrel, deux régimes antiplaquettes. L'étude a révélé une diminution de 16% de risque de crise cardiaque, de course, ou de mort dans le groupe prenant Ticagrelor comparé à ceux qui a pris le clopidogrel. L'étude de PLATON a démontré les avantages de Ticagrelor pour la survie des malades, et actuellement est largement recommandée comme stratégie de traitement pour ACS. En outre, en même temps elle réduit l'infarctus du myocarde effectif et thrombose après implantation de stent, elle également n'augmente pas le risque global de saignement mortel et d'autres effets inverses sérieux. Ticagrelor cependant a deux points faibles. D'abord, il doit être pris deux fois par jour, comparé à une fois par jour pour le clopidogrel, et deuxièmement, il peut causer des effets inverses tels que des difficultés de respiration, sensiblement plus qu'avec ce dernier. Sa demi vie est seulement 12 heures, et pris deux fois par jour, un défi pour des patients présentant la conformité pauvre. Dans la pratique, on l'a également constaté qu'environ 20% de patients soignés avec le clopidogrel ne suivent pas leurs prescriptions, et ces patients sont même moins pour prendre les doses prescrites en utilisant le ticagrelor. Ainsi, à mesure qu'une drogue rapidement réversible, le retrait direct augmentera vraisemblablement le risque de thrombose aiguë, entraînant l'infection ou la course myocardique. |
| Description | En décembre 2010, le ticagrelord'antagoniste de récepteur de P2Y12 (également connu sous le nom d'AZD6140) a été approuvé en Europe pour le traitement du syndrome coronaire aigu (ACS), une condition qui couvre plusieurs symptômes cliniques de potentiel de causer l'ischémie myocardique aiguë (MI). Grippages d'ADP à deux récepteurs purinergiques, aux récepteurs de P2Y1 etde P2Y12. L'action de l'attache d'ADP aux résultatsde récepteur de P2Y12 dans l'activation du ⅢⅡ a du Ⅱ b du Ⅲ a (integrin) receptor.GP du généraliste b lance et prolonge l'agrégation de plaquette, qui a consécutivement comme conséquence l'édition absolue des plaquettes par la formation de fibrine et finalement de thrombus. L'inhibition de la stimulation d'ADP du récepteurde P2Y12 s'est avérée une stratégie efficace pour contrôler les événements atherothrombotic liés à ACS et résulter potentiellement de l'intervention coronaire percutanée (PCI, implantation de stent). |
| Propriétés chimiques | Solide blanc |
| Créateur | Astra-Zeneca (Royaume-Uni) |
| Utilisations | Ticagrelor, le premier antagoniste oral réversible du récepteur P2Y12, fournit plus rapidement, plus grande, et plus cohérente inhibition d'ADP-récepteur que Clopidogrel. Utilisé dans le traitement des syndromes coronaires aigus (ACS) |
| Utilisations | Ticagrelor est le premier réversiblement antagoniste oral obligatoire du récepteur P2Y12, empêche également CYP2C9 et hydroxylation 4 avec IC50 le μM 10,5 du μM et 8,2 respectivement |
| Définition | ChEBI : Un triazolopyrimidine qui est un isostere d'adénosine ; l'anneau de cyclopentane est semblable au ribose et [les 1,2,3] parties riche en azote de pyrimidine du triazolo [4,5-d] ressemblent à l'adénine de nucleobase. Un inhibiteur d'agrégation de plaquette qui est employé pour l'evention de p des événements thromboembolic dans les patients présentant le syndrome coronaire aigu. |
| Marque | Brilique et Possia dans l'Union européenne |
| Utilisation clinique | Ticagrelor, découvert et développé par AstraZeneca, est un antagoniste réversible du récepteur P2Y12 (P2T) du diphosphate d'adénosine de plaquette (ADP) approuvé à l'UE en 2010 et a lancé en à l'Allemagne et au R-U en 2011 pour le traitement des patients présentant les syndromes coronaires aigus (ACS). Il a été approuvé aux États-Unis et le Canada suivant en 2011 des résultats réussis de test clinique dans les patients avec ACS qui l'a montré qu'était supérieur aux drogues de préexistence pour réduire la mort due aux causes vasculaires. Ticagrelor est une drogue orale a indiqué pour l'usage en combination avec l'acide acétylsalicylique (aspirin) pour la prévention des événements atherothrombotic dans les patients adultes avec ACS (angine instable, infarctus du myocarde d'altitude non-St (NSTEMI), ou infarctus du myocarde d'altitude de St (STEMI)). À la différence de son prasugrel et clopidogrel de concurrents, qui exigent le bioactivation, le ticagrelor n'est pas une prodrogue et n'exige pas in vivo l'activation. Il a un début rapide d'action, de réversibilité relativement rapide, de plus grand pouvoir, et de cohérence d'objets exposés dans l'inhibition de plaquette. Après le dosage, le ticagrelor atteint Cmax dans environ 1,5 h, avec la formation d'un métabolite important avec l'activité intrinsèque équipotente au composé de parent. |
| Synthèse chimique | La découverte initiale de la drogue et des études de SAR ont été éditées en 2007, y compris les demandes de brevet initiales de découverte. Depuis lors, un certain nombre de brevets ont été édités avec de diverses améliorations apportées pour la synthèse à grande échelle de la drogue. Tandis que la molécule a été synthétisée utilisant de diverses modifications des intermédiaires communes, le montant à grande échelle de préparation par l'intermédiaire d'une stratégie convergente comportant l'accouplement de trois intermédiaires principales suivant les indications du plan ci-dessous. Plusieurs itinéraires à la synthèse de l'alcool aminé 235 de cyclopentyl ont été rapportés. La plupart de ces itinéraires sont basées sur la réaction de l'acétate 238 de cyclopentene avec de l'amine appropriée, qui est disponible dans le commerce. Intéressant, un itinéraire visant le ticagrelor contenant du deutérium a employé une réaction de Diels-aulne de nitroxide au cyclopentadiene pour incorporer l'amine au système d'anneau. La préparation le plus susceptible de processus-échelle de l'amine principale de cyclopentyl exigée pour le ticagrelor est accentuée dans le plan ci-dessous. L'acétate disponible dans le commerce 238 d'enantiopure a été mis à réagir avec le diimide de Di-tert-butyloxy de sodium dans des conditions palladiummediated catalytiques d'amination pour donner BRI-Boc l'amide 239 dans le rendement de 92%. Dihydroxylation du cyclopentene 239 utilisant le tetraoxide catalytique d'osmium et le N-oxyde n-méthylique de morpholine (NMO) dans THF/water a quantatively eu comme conséquence le cis-diol 240. L'amine libre a été libérée avec du HCL de 6 N suivi du ketalizaion in situ du sel 241 de chlorhydrate de cis-diol dans le rendement de 92%. Le carbamate 242 de Cbz a été quantitativement synthétisé de 241 dans des conditions standard. L'alcool 242 a été préparé avec du t-butoxyde de potassium et l'acétate de bromoethyl (243), l'intermédiaire d'ester dont a été réduit in situ avec de la borohydrure de lithium à l'alcool 244 dans le rendement global de 86% (deux étapes). Hydrogenolysis à la barre 1,2 de la pression d'hydrogène avec 5% Pd/C a donné à alcool aminé 235 intermédiaires dans le rendement de 83%. Cette amine (235) a été mélangée à de l'acide oxalique pour fournir le sel d'oxalate dans le rendement de 82%, qui a été plus tard employé pour la synthèse finale du ticagrelor. La préparation à grande échelle du ticagrelor a rendu nécessaire la synthèse du thioéther 236 de pyrimidine de dichloroamino, pour laquelle il y a plusieurs itinéraires rapportés. La synthèse est lancée avec la construction de l'acide barbiturique 247 de thiol (complotez ci-dessous). Cette intermédiaire a été formée de la réaction du malonate diméthylique (245) avec de la thio-urée (246) en présence du methoxide de sodium. Ces conditions ont fourni le sel de sodium du thiol 247 de pyrimidone dans le rendement de 83%, qui a été isolé par l'intermédiaire de la filtration du mélange de la réaction. Le sel 247 a été alors mis à réagir avec le propyliodide en hydroxyde de sodium méthanolique aqueux suivi du HCL éteignent pour fournir le thioéther désiré 248 dans le rendement de 76%. La nitration du thioéther 248 de pyrimidinol a été réalisée par traitement avec émettre de la vapeur l'acide nitrique en acide acétique, fournissant le pyrimidinol nitro 249 dans le rendement de 75%. La bri-chloruration suivante avec POCl3 a converti 249 en thioéther 250 de dichloropyrimidine dans le rendement quantitatif proche. Dans une publication plus tôt, une réduction sélective du thioéther nitro 250 de dichloropyrimide a été démontrée par l'hydrogénation à la pression d'hydrogène de 3 barres utilisant le catalyseur 3%Pt/0.6%V/C de fournir le thioéther aminé 236 de dichloropyrimidine po ? rendement de 95%. Il est également de note celui pour la réaction plus grande de kilo-échelle, hydrogénation sélective a été accompli avec Pt/V/C (2% pinte ; 1% V sur le catalyseur de carbone) avec la barre 8 de la pression d'hydrogène de donner le thioéther aminé brut 236 de dichloropyrimidine. Tandis qu'un certain nombre d'itinéraires ont été décrits pour la préparation de l'intermédiaire d'amine de cyclopropyl 237,184-187,193-196 que l'itinéraire de large échelle utilisé est décrit (plan ci-dessous) .195 condensation d'acide malonique et le difluorobenzaldehyde 3,4 (251) avec de la pipéridine en pyridine a donné 252 acides dans le rendement de 88% après manoeuvre acide. Le chlorure acide 253 a été préparé utilisant le chlorure de thionyle, qui a été suivi d'estérification avec du L-menthol et la pyridine pour donner l'ester 254 de Lmenthol dans 93% plus de 2 étapes. Cyclopropanation avec le methylide de dimethylsulfoxonium dans DMSO a donné le cyclopropane désiré 255 de transport po ? rendement de 40% et 92% EE après recristallisation. L'hydrolyse de l'ester suivi de la réaction avec du chlorure de thionyle a donné le chlorure acide 257 dans le rendement global de 61% dans deux étapes. Le chlorure acide 257 a été alors mis à réagir avec l'azoture de sodium en présence du carbonate de sodium et du bromure tétrabutylique d'ammonium dans un mélange biphasé de toluène et d'eau pour donner l'intermédiaire d'azoture d'acyle, qui a été immédiatement soumise pour chauffer le toluène pour fournir, après manoeuvre acide, l'amine intermédiaire principale 237 de cyclopropyl dans le rendement de 88% et 92% EE. Cette intermédiaire enantioenriched a été alors mélangée à r (-) - acide mandélique pour fournir le sel acide mandélique de l'amine 237 (258). Avec chacune des trois intermédiaires fournies par les itinéraires mentionnés ci-dessus, l'assemblage final du ticagrelor a été accompli conformément au plan ci-dessous. D'abord, du sel d'oxalate de l'amine 235 de cyclopentyl a été ajouté au thioéther 236 de dichloroaminopyrimidine en présence de la triéthylamine et à la température élevée pour donner à diamine 259 intermédiaires dans le rendement de 88% après cristallisation. La diamine 259 a été alors soumise à la diazotisation avec du nitrite de sodium en acide acétique et toluène à ~30°C, menant à la formation du triazole 260. Cette intermédiaire a été immédiatement mise à réagir avec 258 (sel acide madelic d'amine 237 de cyclopropyl) pour donner l'intermédiaire 261, qui a été plus tard prise en avant à l'étape finale de deprotection. La réaction de 261 ketal avec du HCL concentré en méthanol et toluène à 15°C a fourni le ticagrelor (XXII) dans le rendement 82-90% au-dessus des 3 étapes |